Рено паренхиматозный характер гематурии диагностика
Добавил пользователь Дмитрий К. Обновлено: 19.09.2024
Под гематурией понимают наличие эритроцитов в моче. Всегда ли это указывает на патологию? Может ли наблюдаться эритроцитурия в норме? Если да, то в каком количестве и как часто? На эти вопросы нет однозначного ответа.
Под гематурией понимают наличие эритроцитов в моче. Всегда ли это указывает на патологию? Может ли наблюдаться эритроцитурия в норме? Если да, то в каком количестве и как часто? На эти вопросы нет однозначного ответа. Многие считают вариантом нормы наличие единичных эритроцитов в утренней порции мочи, собранной после соответствующего туалета [2, 15, 19]. Вместе с тем дети, у которых даже изредка появляются единичные эритроциты в общем анализе мочи, требуют наблюдения и определенного алгоритма обследования в течение нередко нескольких месяцев.
Рассматривая гематурию как проявление изолированного мочевого синдрома (ИМС), надо учитывать как степень ее выраженности, так и возможность сочетания ее с другими изменениями в анализе мочи и, прежде всего, с протеинурией.
Следует различать гематурию и по продолжительности. Она может быть кратковременной (например, при прохождении камня), иметь интермиттирующее течение, как это бывает при болезни Берже — одном из вариантов IgA-нефропатии, а также характеризоваться стойким, упорным течением, сохраняя различную степень выраженности на протяжении многих месяцев и даже лет (различные варианты гломерулонефрита, наследственный нефрит, некоторые виды дисплазии почки). Она может быть бессимптомной (при ряде врожденных и наследственных заболеваний почек) либо сопровождаться дизурией или болевым синдромом (при почечной колике).
Клубочковая гематурия (табл. 1), как проявление ИМС, встречается преимущественно при невоспалительных повреждениях гломерулярных капилляров; точнее, при отсутствии сколько-нибудь выраженной пролиферативной реакции со стороны мезангия. Исключением является лишь IgA-нефропатия, которая долгое время может протекать без каких-либо экстраренальных проявлений. Заболевания, при которых гематурия сопровождается экстраренальными симптомами, морфологически имеют выраженный пролиферативный характер воспалительной реакции либо преимущественно со стороны мезангия, либо со стороны эндотелиальной выстилки капилляров клубочка.
Канальцевая гематурия наблюдается при разнообразных заболеваниях как врожденного, так и приобретенного происхождения (табл. 2).
Механизм возникновения почечной гематурии. До сегодняшнего дня нет единого представления о патогенезе почечной гематурии. Само собой разумеется, что эритроциты могут попасть в мочевое пространство почки лишь из капиллярного русла, и гематурию при почечной патологии традиционно связывают с повреждением клубочковых капилляров. При микрогематурии эритроциты проходят через анатомические поры в базальной мембране из-за ее повышенной проницаемости [7, 23]. Макрогематурия обусловлена скорее за счет некроза гломерулярных петель [9, 14, 20, 22, 23]. Причиной гематурии может быть истончение базальной мембраны с нарушением структуры коллагена IV типа и уменьшение в составе ее плотного слоя содержания ламинина, что характерно для наследственного нефрита [5, 7].
Считается более вероятным, что главным местом проникновения эритроцитов через капиллярную стенку является клубочек. Этому способствует имеющееся в клубочке повышенное внутрикапиллярное гидростатическое давление, под влиянием которого эритроциты, меняя свою конфигурацию, проходят через существующие поры [18, 22]. Проницаемость для эритроцитов усиливается при нарушении целостности базальной мембраны, что происходит при иммуновоспалительном поражении стенки капилляра. Некоторые авторы в возникновении гематурии не исключают нарушения морфофункциональных свойств эритроцитов, в частности, снижения их заряда [6]. Вместе с тем отсутствует корреляция между выраженностью изменений в клубочках и степенью гематурии [11]. Этот факт, а также часто отсутствие выраженной гематурии при нефротическом синдроме, когда бывает резко нарушена структура базальной мембраны, дали основание ряду авторов высказать иную точку зрения на механизм гематурии, а именно — основным местом выхода эритроцитов являются перитубулярные капилляры [10, 11]. Эти капилляры в отличие от гломерулярных не имеют эпителиального слоя и очень тесно соприкасаются с канальцевым эпителием; при этом обнаруживаются часто значительные изменения дистрофического характера как в эндотелиальных клетках капилляров, так и в эпителии канальцев [11].
Несмотря на существующую неясность природы почечной гематурии при нефропатиях, тем не менее, важно знать место ее возникновения — клубочек или каналец. Дисморфизм эритроцитов, обнаруживаемый при фазово-контрастной микроскопии, дает возможность отличить почечную гематурию от внепочечной [4, 8, 9, 25, 26], но не позволяет дифференцировать гломерулярную эритроцитурию от перитубулярной [11, 16, 21, 27]. На канальцевую или перитубулярную гематурию может указывать появление в моче плазменных низкомолекулярных белков, обычно полностью реабсорбируемых в проксимальном канальце. К таким белкам относится бета2-микроглобулин (бета2-МГ). Если при гематурии обнаруживается в моче бета2-МГ в количестве, превышающем 100 mг при отсутствии или меньшем количестве в ней альбумина, то такую гематурию следует расценивать как канальцевую [24]. Другими маркерами канальцевой гематурии могут быть ретинолсвязывающий белок [12] и альфа1-микроглобулин [17, 28]. Определение последних предпочтительней, т. к. бета2-МГ легко разрушается в очень кислой моче.
Диагностика гематурии у детей. Диагностика бессимптомной гематурии представляет для врача наибольшие трудности. Однако отсутствие той или иной симптоматики на данный момент не исключает наличие ее в анамнезе, как, например, имевшие место в прошлом болевой синдром, или дизурия, или подъемы температуры без катаральных явлений. Диагностический процесс, как всегда, должен начинаться со сбора подробного анамнеза. В табл. 3 представлены основные моменты, на которые должно быть обращено внимание врача при сборе анамнеза. Выявление тех или иных особенностей данных анамнеза позволит наиболее рационально провести обследование больного, а анализ обстоятельств, при которых была выявлена гематурия, поможет его упростить.
Чрезвычайно важно определить возраст, когда имел место дебют гематурии, ибо установление факта появления гематурии в раннем детском возрасте позволяет рассматривать ее как проявление чаще всего какой-либо врожденной или наследственной патологии. Утвердиться в этом позволит тщательно изученные семейный и акушерский анамнезы. Важно установить, является ли гематурия постоянной или возникает эпизодически на фоне какого-либо интеркуррентного заболевания, охлаждения или физической нагрузки. Определенное значение имеет и выраженность ее, т. е. проявляется она макро- или микрогематурией. Но большую значимость следует придавать сопутствующей ей протеинурии, особенно когда она имеет постоянный характер. Это всегда указывает на почечное происхождение гематурии.
Приступая в условиях поликлиники к обследованию ребенка с выявленной гематурией, прежде всего, необходимо определить место ее возникновения, т. е. является ли гематурия почечной или она внепочечная. Несомненно, если гематурия сопровождается протеинурией, то не почечное ее происхождение исключается. При отсутствии протеинурии первым этапом в обследовании должно быть проведение двухстаканной пробы (см. схему 1 на стр. 56). Обнаружение эритроцитов только в первой порции указывает на наружное их происхождение. В этом случае осмотр наружных гениталий, взятие мазков на микроскопию и скрытую инфекцию, соскоба на энтеробиоз поможет выявить воспалительный процесс и его причину. При обнаружении признаков воспаления необходимо исключить аллергический его характер. Для этого помимо получения соответствующих анамнестических данных следует назначить вульво- или уроцитограмму, которая при наличии превалирования лимфоцитов и обнаружении эозинофилов позволит исключить бактериальный характер воспалительного процесса. Обнаружение эритроцитов в двух порциях свидетельствует о вовлечении в патологический процесс почек и/или мочевого пузыря. Патологию со стороны мочевого пузыря можно заподозрить, помимо соответствующих анамнестических данных, при ультразвуковом исследовании, но только цистоскопия дает возможность окончательно удостовериться в наличии или отсутствии цистита. Ультразвуковое исследование (УЗИ) позволяет выявить изменения положения формы и размера почек, предположить возможность наличия цистита, а также нейрогенного мочевого пузыря. Кроме того, при помощи УЗИ можно обнаружить наличие конкрементов. Последующее проведение в/в урографии и/или реносцинтиграфии поможет уточнить характер выявленных изменений.
Гематурия, сочетающаяся с протеинурией, как уже об этом было сказано, имеет почечное происхождение. В случае установления данной патологии в анализах мочи в раннем детском возрасте, проведя соответствующий сбор анамнеза (табл. 3), следует определить, является ли заболевание врожденным или наследственно обусловленным. Предлагаемый алгоритм действий (см. схему 2 на стр. 57) позволяет на первом этапе не только наметить проведение дифференциальной диагностики между врожденной и наследственной патологией почек, но и подойти к выявлению таких заболеваний, как интерстициальный нефрит и обменная нефропатия, для которых гематурия является одним из проявлений данной патологии.
При появлении гематурии, сочетающейся с протеинурией, в дошкольном и школьном возрастах не исключают наследственную или врожденную природу заболевания. Однако значительно возрастает роль приобретенной патологии в виде различных форм первичного или вторичного гломерулонефрита, интерстициального нефрита, диабетической нефропатии, а также пиелонефрита. После подробного сбора анамнеза обследование этой группы детей следует начинать со сбора суточной мочи на белок и проведения ортостатической пробы. Суточную мочу на белок предпочтительнее собирать раздельно в дневное и ночное время. Это дает возможность оценить значение физической нагрузки на выраженность как протеинурии, так и гематурии. Поскольку у детей этой возрастной группы при сочетании гематурии с протеинурией возрастает частота возникновения различных вариантов гломерулонефрита, необходимо выявить возможную связь этой патологии с гемолитическим стрептококком. Для этого недостаточно обнаружить его наличие путем взятия мазков из зева, необходимо установить появление и нарастание титра антистрептококковых антител (АСЛ-О), а также активацию комплементарной системы.
Обязательным этапом в обследовании этой группы пациентов является проведение УЗИ почек. Несмотря на нормальную ультразвуковую характеристику почек при наличии изолированного мочевого синдрома в виде гематурии с протеинурией, независимо от степени их выраженности, при положительной ортостатической пробе требуется проведение внутривенной урографии. Последняя позволит исключить дистопию почек, наличие их неподвижности, а также окончательно решить вопрос об отсутствии патологической подвижности почек. Из функционального обследования достаточно бывает ограничиться проведением пробы Зимницкого, а для уточнения состояния тубулоинтерстиция — пробы с лазиксом [1]. В случае выявления при УЗИ почек тех или иных отклонений может потребоваться, помимо перечисленного, проведение пробы Реберга, а также реносцинтиграфии.
Таким образом, прежде чем решать вопрос о необходимости применения инвазивных методов обследования у детей с ИМС, проявляющимся в виде гематурии, необходимо провести изложенное выше базисное обследование в амбулаторных условиях. Это позволит, с одной стороны, предотвратить ненужную госпитализацию, а с другой — сократить пребывание детей на специализированной койке, если потребуется более углубленное обследование.
Литература
Архипов В. В., Ривкин А. М. Диагностика функционального состояния почек с использованием фуросемида. Методические рекомендации. СПб, 1996.
Думан В. Л. Фазово-контрастная микроскопия мочевого осадка в дифференциальной диагностике гематурии. Сборник трудов IV ежегодного нефрологического семинара. СПб, 1996, с. 150–152.
Игнатова М. С., Фокеева В. В. Наследственный нефрит: диагноз, патогенез, генетика, прогноз // Клин. мед. 1994, № 2, с. 51–55.
Николаев А. Ю., Щербин А. А. и др. Механизм гематурии при гематурических нефритах // Тер. архив, 1988, № 6, с. 34–37.
Приходина Л. С., Малашина О. А. Современные представления о гематурии у детей // Нефрология и диализ, 2000, № 3, с. 139–145.
Bernard A. M., Moreau D., Lanweys R. Comparison of retinal binding protein and бета2-microglobulin in urine in the early detection of ambular proteinuria // Clin. Chim. Acta. 1982; 126: 1–7.
Birch D. F., Fairley K. F. Haematuria — glomerular or nonglomerular? // Lancet. 1979; vol. 2, p. 845–846.
Bohle A. at al. Morphologic contribution on gross hematuria in mild mesangioproliferative glomerulonephritis without crescents // Klin. Wochenschr. 1985; 63: 371–378.
Dodge W. F., West E. F. et al. Proteinuria and hematuria in schoolchildren: epidemiology and early natural history // J. Pediatrics. 1976; 88: 327–347.
Gibbs D. D., Linn K. J. Red cell volume distribution curves in the diagnosis of glomerular and nonglomerular hematuria // Clin. Nephrol. 1990. 33: 143–147.
Jai-Trung L., Hiroyoshi W., Hiroshi M. et al. Mechanism of hematuria in glomerular disease // Nephron. 1983 Vol. 35. P. 68–72.
Froom P. et al. Significance of microhaematuria in young adults // British Med. J., 1984; vol. 288, p. 20–21.
Kincaid-Smidt P. et al. Acute renal failure and tubular necrosis associated with haematuria due to glomerulonephritis // Clin. Nephrol. 1983; 19: 206–210.
Kitamota Y., Tomita M., Akamine M. et al. Differentiation of hematuria using a uniquely shaped red cell // Nephron. 1993, 64: 32–36.
Lin J. T. et al. Mechanism of hematuria in glomerular disease. An electron microscopic study in a case of diffuse membranous glomerulonephritis // Nephron. 1983, 35: 68–72.
Mouradian J. A., Sherman R. L. Passage of erythrocyte throuhg a glomerular basement membrane gap // N. Engl. J. Med. 1975, 293 (18): 940–941.
Peterson P. A. et al. Differentiation of glomerular, tubular and normal proteinuria: determinations of urinary excretion of бета2-microglobulin, albumin and total protein // J. Clin. Invest. 1969, 48: 1189–1198.
Rizzoni G. et al. Evaluation of gomerular and nonglomerular hematuria by phase contrast microscopy // J. Pediatrics. 1983, 103: 370–371.
Sandoz P. Verbesserte Urinsedimentdiagnostik durch Differenzierung der Eritrozytenmorphologie // Ther. Umschau. 1988, 12: 851–856.
Stapleton F. B. Morphology of urinary red blood cells: a simple guide in localizing the site of hematuria // Pediatr. Clin. North Am. 1987, 34 (2): 561–569.
Yu H. et al. Alpha-1 microglobulin: an indicator protein for renal tubula function // J. Clin. Pathol. 1983, 36: 253–259.
А. М. Ривкин, кандидат медицинских наук, доцент
Н. А. Лисовая, кандидат медицинских наук
СПбГПМА, Санкт-Петербург
Мочевой синдром – это лабораторный синдром, который включает протеинурию, гематурию, лейкоцитурию и цилиндрурию. Перечисленные нарушения возникают все вместе либо проявляются в разнообразных сочетаниях из 2-3 признаков. Патология наблюдается при гломерулонефритах, пиелонефритах, мочекаменной болезни и других видах поражения почек. Основные симптомы: отеки на лице, боли в зоне поясницы или внизу живота, дизурические явления. Для диагностики причины синдрома назначается УЗИ, МРТ почек, рентгенологические исследования (КТ, экскреторная урография, реносцинтиграфия). Лечение подбирается с учетом основного и сопутствующих заболеваний.
МКБ-10


Общие сведения

Причины
Бессимптомный мочевой синдром может иметь физиологическое происхождение, особенно при выявлении изолированной протеинурии. Он развивается при интенсивном физическом и психоэмоциональном напряжении, лихорадочных состояниях, употреблении большого количества белковой пищи. Спектр патологических причин лабораторного синдрома разнообразен, чаще всего изменения мочи возникают при следующих группах заболеваний:
- Гломерулопатии. Болезни, протекающие с поражением клубочкового аппарата, сопровождаются нарушениями почечного фильтра и попаданием в мочу патологических включений. К типичным причинам мочевого синдрома относят гломерулонефрит, диабетическую нефропатию, приобретенный амилоидоз. Среди наследственных болезней выделяют синдром Альпорта, липоидный нефроз.
- Тубулопатии. Повреждение почечных канальцев проявляется нарушениями транспорта органических веществ и электролитов, большим количеством цилиндров в моче. К распространенным вариантам тубулопатии относят некротический нефроз, уратную нефропатию, миеломную нефропатию. У детей патология возникает на фоне синдрома де Тони-Дебре-Фанкони, синдрома Олбрайта.
- Интерстициальные болезни почек. Самой частой почечной причиной массивной лейкоцитурии является пиелонефрит, возникающий при инфицировании бактериальными возбудителями. Разнообразные формы мочевого синдрома типичны для тубуло-интерстициального нефрита, который развивается под влиянием токсинов, инфекций, обменных нарушений.
- Мочекаменная болезнь. Нефролитиаз проявляется кристаллурией – накоплением патологических солей в моче, также для него характерна лейкоцитурия, эритроцитурия. При формировании крупных камней и повреждении слизистой оболочки чашечно-лоханочной системы развивается массивная гематурия, которую необходимо отличать от кровотечения на фоне распада опухоли.
- Урологические заболевания. Мочевой синдром – постоянный спутник циститов и уретритов. Характер и интенсивность изменений лабораторных показателей зависит от особенностей течения, длительности и тяжести заболевания. Интенсивная гематурия может указывать на геморрагический цистит, опухоли мочевого пузыря.
Патогенез
В норме почки имеют анатомический барьер, который включает сложный гломерулярный фильтр, не пропускает крупные молекулы и клетки. Диаметр пор составляет до 4 нм, поэтому сквозь них могут проходить только легкие цепи протеинов. При патологических состояниях поры увеличиваются в размерах, вследствие отложения иммунных комплексов и развития воспаления повышается проницаемость сосудистой стенки для макромолекул.
Механизм формирования гематурии до конца не выяснен. Значительную роль в развитии этот симптома имеет вовлечение мезангия, поражение ткани интерстиция и эпителия извитых канальцев. По данным электронограмм, эритроциты способны изменять свою форму и проникать в мочу через мельчайшие разрывы базальной мембраны. Второй вариант гематурии связан повреждениями слизистой мочевыводящих путей при урологических заболеваниях.

Симптомы мочевого синдрома
Многие болезни, появляющиеся мочевым синдромом, вызывают боли в области поясницы. Пациенты жалуются на тупые ноющие боли при гломерулонефрите и хроническом пиелонефрите, сильные схваткообразные ощущения с иррадиацией в промежность при камнях в почках. Симптомы усиливаются при обильном питье, тряской езде, физической нагрузке. Заболевания мочевых путей проявляются болями в нижних отделах живота при мочевыделении.
Еще один типичный признак поражения мочевыделительной системы – нарушения процесса мочеиспускания. Пациенты отмечают учащение походов в туалет, усиление болей во время процесса, императивные позывы. Характерно изменение количества, цвета и плотности мочи, при гнойно-воспалительных процессах появляется резкий неприятный запах. Красный и бурый оттенок мочи указывает на гематурию, коричневый цвет – симптом желтухи.
Осложнения
Наиболее опасным последствием мочевого синдрома является развитие почечной недостаточности. По патогенезу и клинической симптоматике она бывает острой и хронической. Острая почечная недостаточность (ОПН) отражает некроз эпителия канальцев и тяжелые нарушения кровообращения в органе. При своевременно начатом лечении смертность составляет 10-15%, без оказания медицинской помощи – более 50%, у пациентов с тяжелой сопутствующей патологией – до 80%.
При продолжающихся более 3 месяцев анатомо-функциональных поражениях диагностируется хроническая болезнь почек (ХБП). Это опасное неуклонно прогрессирующее заболевание, которое сопровождается постепенным снижением скорости клубочковой фильтрации (СКФ). Финальной стадией ХБП является терминальная почечная недостаточность, которая зачастую сопровождается жизнеугрожающими сердечно-сосудистыми и инфекционными осложнениями.
Диагностика
Для установления факта мочевого синдрома необходимы показатели стандартного лабораторного анализа. При выявлении патологических отклонений от нормы пациенту требуется обследование у врача-нефролога или уролога для выявления первопричины нарушений. Сначала проводится общеклинический осмотр, пальпация поясницы, сбор анамнеза жизни. Расширенная программа диагностики включает такие виды исследований:
- УЗИ почек. При эхосонографии удается обнаружить локальные участки повышенной эхогенности при камнях и опухолях, либо очаги пониженной плотности – абсцессы, кисты. Диффузные изменения почечной паренхимы наблюдаются при амилоидозе, нефрокальцинозе, ХБП. Увеличение размеров органа типично для ОПН, застойной нефропатии, поликистоза.
- Экскреторная урография. Рентгенконтрастное исследование используется для определения реномегалии, выявления деформации контуров органа, определения признаков врожденных аномалий. Урография показывает признаки пиелонефрита, опухоли, ХБП. По данным рентгенографии можно установить наличие поликистоза, гидронефроза.
- КТ почек. Современный рентгенологический метод исследования используется для уточнения структурных аномалий органа, выявления минимальных изменений, не замеченных при других видах диагностики. Компьютерная томография показана при подозрении на опухоли, врожденные пороки, хронические заболевания. Как альтернатива может назначаться МРТ.
- Реносцинтиграфия. Радионуклидное сканирование – информативный метод определения функциональной активности почек. По скорости накопления и характеру распределения фармпрепарата удается обнаружить признаки нефропатии или почечной недостаточности, оценить эффективность лечения, решить вопрос о необходимости проведения операции.
- Ангиография почечных артерий. Исследование назначается при подозрении на преренальные причины поражения органа, которые связаны с аневризмами, тромбозами, артериовенозными фистулами. Проведение ангиографии также рекомендуется пациентам с сердечно-сосудистыми проблемами.
- Проба Реберга. Определение СКФ по клиренсу эндогенного креатинина используется для установления стадии хронической почечной патологии и подбора оптимальных методов лечения. Дополнительно выполняется коагулограмма, биохимический анализ крови с протеинограммой и липидограммой.

Лечение мочевого синдрома
Фармакотерапия
При подборе методов лечения учитывается основная патология, после устранения которой исчезают патологические изменения, характерные для мочевого синдрома. Пациентам рекомендуется соблюдение диеты с ограничением количества поваренной соли, строгим контролем уровня белка и потребляемой жидкости. Для лечения болезни почек и нормализации функций органа используются следующие группы медикаментов:
- Глюкокортикоиды. Препараты имеют мощное противовоспалительное и иммуносупрессорное действие, поэтому они используются при разных формах гломерулонефрита, интерстициального нефрита, нефропатий на фоне аутоиммунных патологий.
- Антибиотики. Противомикробные препараты применяются при лейкоцитурии для устранения бактериальных инфекций мочевыводящих путей. Они подбираются эмпирически с последующей коррекций терапии по результатам бакпосева мочи.
- Диуретики. Препараты из группы петлевых, тиазидных и калийсберегающих средств назначаются для коррекции водно-солевого баланса, уменьшения почечных отеков, предупреждения кардиоваскулярных осложнений.
- Кардиотропные средства. Во врачебной практике типично сочетание мочевого синдрома с артериальной гипертензией и другими болезнями сердца, поэтому в комплексной терапии применяются гипотензивные, гиполипидемические, кардиометаболические лекарства.
Экстракорпоральные методы детоксикации
Для коррекции системных проявлений почечной недостаточности и замещения утраченной функции органа проводится гемодиализ ежедневно или через день при ОПН, регулярно 1-3 раза в неделю при хроническом заболевании почек. По показаниям применяются другие экстракорпоральные методы: плазмаферез для удаления токсинов и продуктов метаболизма из плазмы крови, процедуры непрерывной терапии (гемофильтрация и гемодиафильтрация).
Хирургическое лечение
При хронической недостаточности функций почек рассматривается возможность радикальных мер – трансплантации органа. Пересадка является наиболее эффективным способом коррекции заболевания, она позволяет значительно продлить жизнь пациентам. Помощь хирургов может потребоваться для коррекции врожденных аномалий развития, нарушающих работу почек, для устранения сосудистых патологий в бассейне почечных артерий.
Прогноз и профилактика
Отдаленные риски для пациента зависят от первопричины отклонений в анализе мочи и правильности лечения. При отсутствии признаков почечной недостаточности и других соматических заболеваний удается полностью ликвидировать проблему методами консервативного лечения. После перенесенной ОПН до 50% выздоровевших имеют снижение функций почек, около 5% нуждаются в постоянной почечно-заместительной терапии. ХПН требует пожизненного поддерживающего лечения.
Поскольку мочевой синдром не является самостоятельной нозологией, суть превентивных мер сводится к предупреждению развития болезней почек. Пациентам рекомендуется придерживаться здорового питания с ограничением жиров и соли, избегать переохлаждений, своевременно лечить инфекции нижних мочевыводящих путей. Для профилактики токсических поражений почек врачам необходимо рационально подходить к подбору фармакотерапии, избегать полипрагмазии.
4. Мочевой синдром: диагностический поиск/ Е.В. Архипов, О.Н. Сигитова// Вестник современной клинической медицины. – 2012. – №4.
Классификация
По характеру выделяют следующие виды гематурии:
- Физиологическую (функциональную). Гематурия может выявляться у абсолютно здоровых людей во многих случаях. У детей младшего возраста гематурия обусловлена повышенной проницаемостью незрелого почечного фильтра. У взрослых гематурия отмечается после перегревания, переохлаждения, проверки симптома Пастернацкого, интенсивных физических нагрузок или длительных пеших переходов (маршевая гематурия).
- Патологическую (органическую). Органическая гематурия связана с различными патологическими процессами – заболеваниями почек инфекционного или аутоиммунного генеза, наличием конкрементов в мочевыводящих путях, болезнями с нарушением свертывания крови и т.д.
По степени выраженности различают:
- Микрогематурию. Встречается наиболее часто. Визуально моча не изменена. Эритроциты обнаруживаются только во время микроскопического исследования.
- Макрогематурию. Появление в моче большого количества эритроцитов, которая приобретает характерную окраску. Благодаря этому гематурию можно заподозрить уже при осмотре мочи невооруженным глазом.
По происхождению гематурии подразделяют на:
- Ренальные. Наиболее распространенная форма. Кровь в моче появляется вследствие различных заболеваний почек – пиелонефрита, гломерулонефритов, опухолей почек.
- Преренальные. Наличие в моче крови обусловлено врожденными или приобретенными коагулопатиями – иммунной тромбоцитопенией, гемофилией, длительным прием антиагрегантов или антикоагулянтов.
- Постренальные. Гематурия возникает при патологии нижних отделов мочевыводящей системы – наличии конкрементов, полипоза мочевого пузыря, геморрагического цистита.
При исследовании физико-химических свойств мочи с помощью тест-полосок возможно получение ложных результатов на кровь:
- Ложноотрицательные. Отрицательный анализ мочи на кровь может быть получен при недостаточном перемешивании образца мочи, высокой концентрации аскорбиновой кислоты.
- Ложноположительные. Ложная гематурия возникает в случае присутствия в моче бактерий, содержащих фермент пероксидазу, осаждения на стенках посуды для сбора мочи дезинфектантов с гипохлоритом, при попадании в мочу антисептика бетадина. Также нередкой причиной ложной гематурии является нарушение преаналитического этапа, например, сдача анализа мочи во время менструальных кровотечений.

Причины ренальной гематурии
Гломерулонефриты
Основная причина появления крови в моче у детей. При гломерулонефритах эритроциты попадают в мочу через поврежденную воспалительным процессом стенку капилляров клубочков почек. При прохождении через гломерулярные капилляры клетки крови деформируются, что считается характерным признаком при микроскопии мочи. При хронических гломерулонефритах отмечается умеренная или незначительная гематурия.
При обострении воспаления количество эритроцитов в моче очень высокое, вплоть до макрогематурии с изменением цвета мочи. Часто наблюдается сочетание с лейкоцитурией и протеинурией. После проведения специфической терапии гематурия достаточно быстро исчезает. К патологиям клубочков относятся:
- Постстрептококковый гломерулонефрит.
- IgA-нефропатия (болезнь Берже).
- Гломерулонефриты при коллагенозах: люпус-нефрит при системной красной волчанке, склеродермическая почка при системной склеродермии.
- Гломерулонефриты при системных васкулитах:геморрагический васкулит Шенлейн-Геноха, узелковый полиартериит, гранулематоз Вегенера.
- Поражение почек при гепатите В и С.
Пиелонефрит
Гематурия отмечается приблизительно у 30% больных с острым или обострением хронического пиелонефрита. Воспалительный процесс в почечной лоханке приводит к попаданию крови в почечные канальцы. Однако количество эритроцитов незначительное либо умеренное (до 15-20). Гематурии всегда сопутствует лейкоцитурия, бактериурия, положительный тест на нитриты. После антибактериальной терапии кровь, как правило, в моче не обнаруживается.
Некротические поражения почек
Разрушение почечной ткани некротического характера сопровождается выраженной гематурией. Данное состояние может быть вызвано острым тромбозом почечных вен, эмболией почечной артерии тромботическими массами, образующихся в полостях сердца при фибрилляции предсердий или инфекционном эндокардите. Также встречается папиллярный некроз – специфическое осложнение тяжело протекающего пиелонефрита у больных сахарным диабетом.
Гематурия возникает, как правило, остро, на фоне тупой или ноющей боли в пояснице, сочетается с лейкоцитурией. После проведения тромболитической, антикоагулянтной терапии, хирургического удаления тромба или целой почки, некоторое время в моче может присутствовать незначительное количество крови.
Другие причины
- Поликистоз почек;
- Туберкулез почек;
- Опухоль почки;
- Тубулоинтерстициальные нефропатии;
- Врожденные анатомические дефекты мочевыводящей системы;
- Гемолитико-уремический синдром;
- Эссенциальная криоглобулинемия;
- Синдром Альпорта.
Причины постренальной гематурии
Мочекаменная болезнь
Наиболее распространенная причина гематурии у взрослых. Механизм возникновения гематурии при МКБ связан с травматизацией конкрементом почечной лоханки или стенки мочеточника. Кровь появляется во время приступа почечной колики, сопровождающейся выраженным болевым синдромом, тошнотой, рвотой. Степень гематурии зависит от объема повреждения.
При микроскопии часто выявляется большое количество различных кристаллов – оксалатов кальция, фосфатов, кристаллов мочекислого аммония, мочевой кислоты. Вследствие образовавшегося препятствия оттоку мочи, нередко присоединяется инфекция, о чем свидетельствует обнаружение в моче лейкоцитов и бактерий. Вне приступа кровь обычно отсутствует. Гематурия полностью прекращается после хирургического удаления конкрементов.
Заболевания нижних мочевыводящих путей
Гематурия при циститах встречается достаточно редко, чаще она отмечается при полипозах или камнях мочевого пузыря. Возможен геморрагический цистит с выраженной гематурией – при шистосомозе (паразитарная инвазия) мочевого пузыря или как неблагоприятная побочная реакция на длительное применение цитостатического лекарственного препарата циклофосфамида.
При опухоли мочевого пузыря гематурия считается постоянным симптомом, а у людей, страдающих воспалением предстательной железы или мочеиспускательного канала (простатит, уретрит), встречается чрезвычайно редко. В данном случае гематурия сопровождается лейкоцитурией, иногда бактериурией.
Причины преренальной гематурии
Присутствие в моче красных кровяных клеток может быть связано с нарушением работы свертывающей системы крови. К ним относятся врожденные или приобретенные коагулопатии (тромботическая тромбоцитопеническая пурпура, иммунная тромбоцитопения и другие геморрагические диатезы), в т.ч. на фоне применения лекарственных препаратов (антикоагулянтов, антиагрегантов).
Также кровь попадает в мочу вследствие повышенного гидростатического давления в почечных сосудах, которое возникает при сердечно-сосудистых заболеваниях – хронической сердечной недостаточности и злокачественной артериальной гипертензии. Застойная гематурия быстро стихает после улучшения насосной функции сердца и нормализации артериального давления.

Диагностика
При обнаружении гематурии необходимо обязательно обратиться к врачу-терапевту, нефрологу или урологу для выяснения причины ее развития. Огромное значение в дифференциальной диагностике этиологического фактора имеют физикальные и анамнестические данные. Уточняется, не предшествовала ли появлению гематурии инфекция верхних дыхательных путей, какие лекарственные препараты принимает больной, какими хроническими заболеваниями страдает.
Врач проводит осмотр кожных покровов, определяет наличие отеков, измеряет артериальное давление, температуру тела, выполняет аускультацию сердца, спрашивает о болях в пояснице, проверяет симптом Пастернацкого. Для уточнения локализации участка кровотечения проводиться 3-стаканная проба: преобладание крови в 1 порции мочи свидетельствует о поражении уретры или простаты, во 2 – о поражении мочевого пузыря, в 3 или во всех порциях– о почечной гематурии.
При ОАМ обращается внимание на наличие других изменений – лейкоцитурии, протеинурии, бактериурии. При микроскопическом исследовании осадка мочи определяется соотношение неизмененных и дисморфных эритроцитов. Наличие более 75-80% эритроцитов с измененной морфологией говорит о поражении клубочков почек. Также в пользу гломерулярной патологии указывает обнаружение эритроцитарных цилиндров, акантоцитов.
Если при проведении общего анализа мочи отмечается положительная реакция на кровь тест-полосками, а при микроскопии эритроциты не обнаруживаются, может потребоваться дифференциальный диагноз с гемоглобинурией и миоглобинурией, потому что реагентная зона тест-полосок одинаково чувствительна к эритроцитам, к свободному гемоглобину и миоглобину. Назначаются дополнительные методы исследования:
- Анализы крови. В общем анализе крови измеряется уровень гемоглобина, СОЭ, форменных элементов (тромбоцитов, лейкоцитов, эритроцитов), в биохимическом анализе крови – концентрация мочевины, креатинина, СРБ, производится расчет СКФ. В коагулограмме исследуются показатели свертывания крови.
- Иммунологические исследования. При подозрении на постстрептококковый гломерулонефрит назначается анализ на антистрептолизин-О. Для подтверждения коллагенозов требуется обнаружение аутоантител – к двуспиральной ДНК, топоизомеразе, к цитоплазме нейтрофилов.
- Микробиологические исследования. Для идентификации возбудителя при пиелонефрите, цистите или инфицировании почечных камней назначается бактериальный посев с определением чувствительности к антибиотикам.
- УЗИ. При пиелонефрите на УЗИ почек визуализируется расширение чашечно-лоханочной системы, при МКБ – наличие конкрементов. При простатите УЗИ предстательной железы показывает увеличение ее размеров, снижение ее эхогенности. Режим допплера позволяет оценить состояние почечного кровотока.
- Экскреторная урография. На основании рентгенографии после введения контрастного вещества можно выявить обструкцию МВП, что может свидетельствовать о МКБ, полипах, опухоли, аномалиях строения МВП.
- Цистоскопия. Для уточнения характера поражения мочевого пузыря (интерстициальный цистит, опухоль, полип) некоторым пациентам назначается цистоскопия.
- Гистологические исследования. С целью установления точной разновидности гломерулонефрита (мембранопролиферативный, мезангиопролиферативный и пр.) выполняется биопсия почки. Морфологическое исследование показано и в тех случаях, если подозревается злокачественное новообразование или системный васкулит.
Коррекция
Консервативная терапия
Самостоятельных методов коррекции гематурии не существует. Для устранения этого лабораторного феномена необходимо проведение терапии основного заболевания. В случае развития гематурии на фоне приема антикоагулянта, рекомендуется снижение дозировки либо полная его отмена. В качестве консервативной терапии применяются следующие лекарственные препараты:
- Антибиотики. Для лечения пиелонефрита препаратами первой линии выступают пенициллины, цефалоспорины. При цистите назначается фосфомицина трометамол. При простатите эффективны фторхинолоны, макролиды.
- Глюкокортикостероиды. Препараты гормонов коры надпочечников (преднизолон) способны подавлять выраженность воспаления в гломерулярном аппарате и аутоиммунное разрушение тромбоцитов при геморрагических диатезах.
- Цитостатики. К цитостатическим средствам (азатиоприн, циклоспорин) прибегают при тяжелом течении гломерулонефритов, особенно при васкулитах и коллагенозах. Также комбинации из химиотерапевтичеких ЛС назначаются при опухолях почки, мочевого пузыря.
- Альфа-адреноблокаторы (тамсулозин). Данная группа препаратов оказывает расслабляющий эффект на стенки мочеточников и сфинктеры мочевого пузыря, что способствует самостоятельному отхождению конкрементов небольшого размера.
- Щелочные растворы. Для растворения камней мочевой кислоты используются цитрат калия или бикарбонат натрия.
- Кардиологические препараты. Пациентам с хронической сердечной недостаточностью и артериальной гипертензией назначаются бета-адреноблокаторы, ингибиторы АПФ, калийсберегающие диуретики.
Хирургическое лечение
Больным с МКБ выполняется ударно-волновая литотрипсия или лапароскопическое удаление камней, при поликистозе, доброкачественной опухоли, инфаркте почки – резекция, наложение нефростомы или тотальная нефрэктомия. При выраженном двустороннем поражении почечной ткани с развитием терминальной почечной недостаточности по жизненным показаниям может быть проведена трансплантация почки.
Прогноз
Гематурия – довольно серьезный клинико-лабораторный признак, при обнаружении которого следует немедленно обратиться к специалисту. Прогноз для жизни определяется тем заболеванием, при котором в моче появилась кровь – наиболее благоприятный при цистите или простатите и крайне неблагоприятный при быстропрогрессирующем гломерулонефрите или опухоли почки.
1. Дифференциальный диагноз внутренних болезней: Алгоритмический подход/ Хили П.М., Джекобсон Э.Дж. - 2014
4. Клиническая лабораторная диагностика : уч.- метод. пособие для студентов лечебного, педиатрического и медико-психологического факультетов / С.В. Лелевич, В.В. Воробьев, Т.Н. Гриневич – Гродно : ГрГМУ, 2011. – 166 с
МКБ-10

Общие сведения
Ангиолипома почки представляет собой доброкачественную опухоль, включающую в себя сосуды, жировую ткань и некоторое количество гладкомышечных клеток. Последнее обстоятельство стало основанием для синонимического названия данного образования – ангиомиолипома. Является достаточно распространенным опухолевым поражением выделительной системы, однако точные статистические данные неизвестны по причине большого количества бессимптомных форм патологии.

Причины
Этиология ангиолипомы почки остается невыясненной, достоверно даже неизвестно, имеет ли она врожденный или приобретенный характер. Удалось установить взаимосвязь между развитием опухоли и некоторыми генетическими заболеваниями (туберозный склероз), однако клиническое течение этих форм значительно отличается от спорадических образований. На основании многолетнего изучения множества больных было предложено несколько возможных механизмов развития ангиолипомы и теорий относительно причин ее возникновения:
- Хроническое воспаление. Новообразование довольно часто сочетается с хроническим гломерулонефритом, пиелонефритом, мочекаменной болезнью, что свидетельствует о возможном влиянии воспаления на процесс развития патологии. Противники этого мнения указывают, что сама опухоль может стать первичным провоцирующим фактором этих состояний.
- Влияние эндокринных сбоев. Ангиолипома почек часто регистрируется у женщин в климактерический период, когда возникают глобальные гормональные перестройки в организме. Описаны случаи резкого ускорения роста образования при беременности, что также объясняется влиянием изменившегося гормонального фона. Однако вызывают ли такие изменения опухоль почки или стимулируют рост уже имеющейся – достоверно не выяснено.
- Наследственный фактор. Патология сопровождает как минимум одно генетическое заболевание – болезнь Бурневилля-Прингла, при которой возникают множественные ангиолипомы в обеих почках. Относительно спорадических форм четкой наследственной передачи зафиксировать не удалось.
- Вирусная этиология. Предполагается, что опухолевый рост такого типа может стимулироваться определенным типом вирусов. Но на сегодняшний день данная теория не подтверждена экспериментально.
В научной среде существует общепризнанное мнение относительно основных факторов риска возникновения данной опухоли, в число которых входит женский пол, беременность, климактерический период, гормональные сбои, повышенный уровень женских половых гормонов у мужчин. Сочетание этих обстоятельств с воспалительными или метаболическими поражениями органов выделительной системы значительно увеличивает вероятность развития доброкачественного новообразования.
Патогенез
Увеличение ангиолипомы свыше 40-50 мм приводит к сдавлению нервных стволов, из-за чего возникает болевой синдром. Опухолевые сосуды несостоятельны и часто повреждаются, кровь из них попадает сначала в чашечно-лоханочную систему почки, а оттуда в мочу, приводя к развитию гематурии. При значительных размерах новообразования в случае механических нагрузок (резкие движения, поднятие тяжестей) может произойти разрыв опухоли с возникновением кровотечения. Состояние сопровождается выраженной анемией, сильными опоясывающими болями в животе, ригидностью мышц брюшного пресса и требует срочного хирургического вмешательства.
Классификация
Широкая распространенность патологии на фоне мало выясненных причин ее развития стала поводом для разработки многочисленных систем классификации – на основе чувствительности к гормонам, наличия инвазивного роста, возраста появления и других критериев. Ни одна из перечисленных систем не получила широкого и общепризнанного распространения, так как они обладают массой недостатков. В современной урологии используют только одну классификацию ангиолипомы почки, где за основу взят известный этиологический фактор ее развития:
- Спорадический тип. Является наиболее распространенным, составляет 75-80% всех случаев заболевания. Неоплазия определяется при случайном ультразвуковом исследовании органов мочевыделительной системы, имеет небольшие размеры, характеризуется экспансивным ростом, бессимптомным течением. Поражение всегда одностороннее, образование одиночное.
- Наследственный тип. Включает опухоли, сопровождающие генетические заболевания. Обычно это синдром Бурневилля-Прингла (туберозный склероз) – аутосомно-генетическая патология из группы факоматозов. Она сопровождается множественными двухсторонними ангиомиолипомами почек и обуславливает примерно 20% случаев таких образований.
- Тип с невыясненной этиологией. Диагностируется редко (примерно 1-5% случаев), включает в себя все остальные виды ангиолипом выделительной системы. К нему относят множественные спорадические новообразования, опухоли с инвазивным ростом, неоплазии, сопровождающие другие онкологические заболевания почек.
Симптомы ангиолипомы почки
Из-за отсутствия болевых рецепторов в паренхиме почки для заболевания характерно преимущественно бессимптомное течение. Известны случаи артериальной гипертензии почечного генеза у больных с небольшими по размерам новообразованиями, но она может быть обусловлена другими механизмами. Явная симптоматика появляется в тот момент, когда опухоль начинает оказывать давление на капсулу почки, снабженную нервными окончаниями. Это проявляется длительными тянущими болями в пояснице, поначалу без определенной иррадиации в какую-либо сторону. По мере прогрессирования ангиолипомы почки боль концентрируется на стороне пораженного органа.
Одновременно с болевым синдромом возникает гематурия, которая сначала определяется только при лабораторном изучении мочи, а затем становится видна невооруженным глазом. Длительное течение заболевания приводит к развитию анемии и гипоальбуминемии. Иногда наблюдается затруднение оттока мочи вследствие блокировки участком ангиомиолипомы с развитием почечной колики. Резкое усиление боли, ее распространение на всю область живота, бледность и тахикардия являются признаками разрыва новообразования и забрюшинного кровотечения. При таких симптомах больного необходимо срочно доставить стационар для оказания хирургической помощи.
Продолжительность течения патологии велика – бессимптомная стадия может занимать много лет, длиться вплоть до смерти больного по естественным причинам. Период от появления первых болезненных ощущений до возникновения макрогематурии также занимает много месяцев и даже лет. Медленное прогрессирование и незначительность проявлений ангиомиолипомы, с одной стороны, позволяют назначать длительное наблюдение вместо хирургического лечения, а с другой – приводят к позднему обращению больных к специалисту.
Осложнения
Самым частым осложнением ангиолипомы почки является разрыв опухоли – неоплазия богата сосудами с хрупкими стенками, поэтому их повреждение приводит к обильным, долго не останавливающимся кровотечениям. Кровоизлияние происходит в забрюшинное пространство или (реже) в ЧЛС, проявляется гематурией, грозит развитием шока в результате кровопотери и раздражения брюшины. Редкой формой отдаленного осложнения патологии является малигнизация опухоли – она приобретает инвазивный характер роста и способность к метастазированию. В результате прорастания стенки венозных сосудов возможна их эмболия и нарушения кровообращения в почках.
Диагностика
Определением наличия новообразования и его типа занимается врач-уролог в тесной кооперации с онкологом. Часто ангиолипома почки выявляется случайно в ходе профилактического ультразвукового исследования или других диагностических манипуляций, при которых оценивается структура органов выделения. Для уточнения характера образования, его размеров, локализации, взаимоотношений с окружающими тканями используется целый ряд методик:
- Пальпаторное исследование. Если ангиомиолипома имеет размеры свыше 5-ти сантиметров, ее можно обнаружить при обычной пальпации почек больного. Кроме подтверждения наличия неоплазии никаких других данных этот метод не дает.
- Ультразвуковые исследования. УЗИ почек обнаруживает опухоль в виде однородного эхогенного образования различных размеров. Посредством допплерографии (УЗДГ почек) можно подтвердить сосудистый характер новообразования, выявить возможные повреждения и разрывы сосудов.
- Мультиспиральная компьютерная томография.МСКТ почек с контрастом является золотым стандартом в определении положения и размеров ангиолипомы. При плановой операции по удалению опухоли такое исследование при отсутствии противопоказаний входит в обязательную предоперационную подготовку.
- Магнитно-резонансная томография.МРТ почек используют как альтернативу МСКТ при подготовке к хирургическому вмешательству или для определения размеров и структуры неоплазии. Ангиомиолипома выявляется как умеренно гиперденсивное округлое образование в почке.
- Биопсия почки и гистологическое изучение. Является эталоном при уточнении характера опухоли, часто используется для окончательного подтверждения диагноза. Забор образцов производится посредством эндоскопического оборудования под контролем УЗИ или рентгеноскопических методик. При микроскопии выявляются сосудистый и жировой компоненты с примесью гладкомышечных волокон.
- Генетическое исследование. Проводится в случае подозрения на наличие туберозного склероза. Диагностика заключается в автоматическом секвенировании последовательностей генов TSC1 и TSC2, мутации которых приводят к развитию болезни Бурневилля-Прингла.

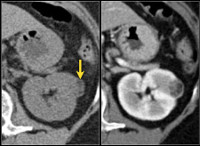
КТ ОБП и забрюшинного пространства. Объемное образование жировой плотности (-80…-90 ед. Хаунсфилда), деформирующее наружный край левой почки
Базовые клинические анализы (исследование крови, мочи, измерение артериального давления, оценка функциональной активности почек) играют второстепенную роль в диагностике патологии. При бессимптомном наличии ангиолипомы почки эти исследования практически не указывают на заболевание. В случае выраженных размеров опухоли в ОАМ обнаруживается гематурия и протеинурия, анализ крови выявляет железодефицитную анемию. Биохимия крови может подтверждать наличие гипоальбуминемии.
Лечение ангиолипомы почки
При размерах ангиомиолипомы мерее 40-50 миллиметров, отсутствии выраженной анемии и гематурии лечение не назначается – рекомендуется только наблюдение у уролога или нефролога один раз в полгода с проведением профилактического УЗИ. Показано соблюдение оптимального питьевого режима, снижение нагрузки на выделительную систему, при наличии сопутствующих заболеваний почек – их правильное полноценное лечение. Если ангиолипома почки имеет значительные размеры или становится причиной нарушений (боли, анемия) – назначается хирургическое удаление новообразования. Тип и объем операции зависят от ряда факторов:
Методика хирургического лечения может видоизменяться в зависимости от размеров ангиолипомы, наличия сопутствующих нарушений, состояния больного. Срочная жизнеспасающая операция по остановке забрюшинного кровотечения на фоне разрыва опухоли также часто сопровождается ее удалением. В редких случаях метастазирования в лимфатические узлы удалению подвергаются и они. Консервативных методов лечения ангиомиолипом почек не существует.
Прогноз и профилактика
Ангиолипома почки характеризуется благоприятным прогнозом из-за своего крайне медленного развития и доброкачественного характера роста. Назначенное после выявления опухоли и подтверждения ее типа наблюдение у нефролога позволяет своевременно обнаружить любые негативные изменения в течении патологии. Благодаря этому хирургическое устранение осуществляется вовремя, до развития тяжелых осложнений. По статистике, оперативное лечение требуется менее трети пациентов от всех наблюдаемых по этому поводу у специалиста. У остальных больных новообразование ничем не проявляет себя на протяжении всей жизни.
2. Ангиомиолипома почки/ Матвеев В. Б., Матвеев Б. П., Волкова М. И.// Вестник РОНЦ им. Н. Н. Блохина РАМН. - 2002.
3. Криоабляция ангиомиолипомы почки/ И.И. Абдуллин, Р.Р. Фатихов, Н.Г. Кешишев, И.А. Шадеркин, Н. Щербинин// Экспериментальная и клиническая урология. - 2010. - №4.
4. Эндоваскулярное и хирургического лечение ангиомиолипомы почки, осложненной кровотечением/ Р.А. Хвастунов, П.В. Мозговой, Р.В. Земцов, С.А. Мелешкин// Волгоградский научно-медицинский журнал. - 2017.
Читайте также:

