1 моль одноатомного газа в цилиндре под поршнем нагревается при постоянном давлении от 1
Добавил пользователь Дмитрий К. Обновлено: 19.09.2024
В гладком закреплённом теплоизолированном горизонтальном цилиндре находится 1 моль идеального одноатомного газа (гелия) при температуре T1 = 300 К, отделённый от окружающей среды — вакуума — теплоизолированным поршнем массой m = 2 кг. Вначале поршень удерживали на месте, а затем придали ему скорость V = 10 м/с, направленную в сторону газа. Чему будет равна среднеквадратичная скорость атомов гелия в момент остановки поршня? Поршень в цилиндре движется без трения.
1. Из условия задачи понятно, что по мере движения поршня в адиабатических условиях газ будет сжиматься и нагреваться, а поршень — тормозиться, вплоть до остановки.
2. В момент остановки, т. е. при максимальном сжатии гелия, вся начальная кинетическая энергия поршня перейдет во внутреннюю энергию гелия.
3. Вначале 1 моль одноатомного гелия обладал внутренней энергией а в конце процесса, согласно закону сохранения энергии,
4. Среднеквадратичная скорость атомов гелия в момент остановки поршня связана с температурой формулой и, таким образом, равна
I) записаны положения теории и физические законы, закономерности, применение которых необходимо для решения задачи выбранным способом;
II) описаны все вновь вводимые в решении буквенные обозначения физических величин (за исключением обозначений констант, указанных в варианте КИМ, обозначений, используемых в условии задачи, и стандартных обозначений величин, используемых при написании физических законов);
Записи, соответствующие пункту II, представлены не в полном объёме или отсутствуют.
В решении имеются лишние записи, не входящие в решение (возможно, неверные), которые не отделены от решения (не зачёркнуты; не заключены в скобки, рамку и т. п.).
В необходимых математических преобразованиях или вычислениях допущены ошибки, и (или) в математических преобразованиях/вычислениях пропущены логически важные шаги.
Представлены только положения и формулы, выражающие физические законы, применение которых необходимо для решения данной задачи, без каких-либо преобразований с их использованием, направленных на решение задачи.
В решении отсутствует ОДНА из исходных формул, необходимая для решения данной задачи (или утверждение, лежащее в основе решения), но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи.
1 моль одноатомного газа в цилиндре под поршнем
В герметичном сосуде объёмом V = 1 литр под поршнем находится 1 моль идеального одноатомного газа при атмосферном давлении p . На рисунке изображена pV-диаграмма, показывающая последовательные переходы этого газа из состояния 1 в состояние 5.
Выберите все верные утверждения на основании анализа представленного графика.
1) Работа газа в процессе 4–5 больше работы газа в процессе 2–3 в 1,5 раза.
2) В процессе перехода 4–5 газ совершил бόльшую работу, чем в процессе перехода 2–3–4.
3) Максимальное изменение ΔT температуры газа произошло в процессе 1–2.
4) Отношение разности температур газа в состояниях 5 и 3 к температуре газа в состоянии 1 равно 23.
5) Отношение температуры газа в состоянии 3 к температуре газа в состоянии 4 равно 1,25.
1) Работа газа численно равна площади под графиком pV-диаграммы.
3) Температура идеального газа равна Посчитаем изменения температур на участках:
Уже получили, что изменение температуры газа в процессе 1–2 не наибольшее.
В некотором процессе 1–2, который проводился с одним молем идеального одноатомного газа, среднеквадратичная скорость молекул газа возросла от u1 = 350 м/с до u2 = 380 м/с. При этом давление p газа в процессе оставалось постоянным, и газ совершил работу A = 292 Дж. Чему равна молярная масса этого газа?
1. Согласно молекулярно-кинетической теории идеального газа, среднеквадратичная скорость его молекул связана с температурой газа формулой
2. Работа газа при изобарическом (согласно условию) процессе равна
3. Из уравнения Клапейрона–Менделеева для одного моля идеального газа получаем, что
4. Таким образом, из записанных уравнений следует, что откуда
Один моль идеального одноатомного газа участвует в некотором процессе, в котором теплоёмкость газа постоянна. В начале этого процесса газ имеет давление 200 кПа и занимает объём 1 л. В ходе процесса газ расширяется до объёма 8 л и его давление становится равным 100 кПа. При этом газ получает от окружающих тел количество теплоты 1,8 кДж. Во сколько раз теплоёмкость газа в этом процессе превышает изохорическую молярную теплоёмкость одноатомного идеального газа?
Температуру в первом и во втором случае можно найти из закона Менделеева — Клапейрона: Тогда разность температур равна Молярная теплоёмкость вычисляется по формуле: Молярная теплоёмкость при постоянном объёме для одноатомного идеального газа равна: Найдём отношение теплоёмкостей:
Один моль идеального одноатомного газа совершает адиабатическое сжатие. Как изменяются в результате такого процесса давление и температура газа?
Для каждой величины определите соответствующий характер изменения:
Запишите в таблицу выбранные цифры для каждой физической величины. Цифры в ответе могут повторяться.
Согласно первому началу термодинамики, переданное газу тепло идет на увеличение его внутренней энергии и на совершение работы против внешних сил: Газ сжимается, значит, он совершает отрицательную работу Процесс сжатия адиабатический, следовательно, теплообмен с окружающей средой отсутствует Таким образом, внутренняя энергия увеличивается Внутренняя энергия идеального газа зависит только от температуры. При увеличении внутренней энергии температура увеличивается. Давление связано с объемом и температурой соотношением Таким образом, при адиабатическом уменьшении объема и увеличении температуры газа давление увеличивается.
На рисунке изображён график зависимости объёма V одного моля идеального одноатомного газа от его температуры T в процессе 1–2. Как в результате перехода из состояния 1 в состояние 2 изменяются внутренняя энергия газа и давление газа?
Для каждой величины определите соответствующий характер изменения:
Запишите в ответ цифры, расположив их в порядке, соответствующем таблице:
Внутренняя энергия идеального газа пропорциональна его температуре. Таким образом, при увеличении температуры, внутренняя энергия увеличивается.
Согласно уравнению перехода давление, объём и абсолютная температура идеального газа связаны соотношением
Из графика видно, что зависимость объема от температуры — квадратичная, т.е. имеет вид
Следовательно, отношение давлений имеет вид:
При переходе из состояния 1 в состояние 2 температура увеличивается, а значит, давление уменьшается.
Два моля идеального одноатомного газа находятся в состоянии 1 (см. рис.) при температуре 200 К. Газ совершает циклический процесс, изображённый на диаграмме. Какое количество теплоты получает газ на участке 1−2 этого циклического процесса? Ответ выразите в килоджоулях и округлите до целого числа.
На участке 1−2 процесс изохорный, поэтому V1 = V2, следовательно, работа газа на участке 1−2 равна 0. По первому закону термодинамики Тогда на участке 1−2 количество теплоты равно изменению внутренней энергии газа. Изменение внутренней энергии одноатомного газа в этом случае равно Давление увеличилось от 0,5p до 5p при постоянном объёме. Следовательно, температура газа увеличилась так же в 10 раз. Значит, T2 = 10T1 = 2000 К. Отсюда
Один моль идеального одноатомного газа совершает процесс 1–2–3, изображенный на рисунке. В процессе 1–2 температура газа постоянна и равна 300 К. Какое количество теплоты получил газ на участке 2–3?
В процессе 2–3 происходит изохорное нагревание газа. Работа газа равна нулю и, согласно первому началу термодинамики, переданное газу тепло в таком процессе идет только на изменение его внутренней энергии
При постоянном объеме для идеального газа выполняется закон Шарля, согласно которому Давление на участке 2–3 увеличилось в 3 раза, а значит, и температура увеличилась в 3 раза и стала равной 900 К.
Найдем количество теплоты, которое получил газ
На рисунке изображён график процесса 1–2–3–4 для двух молей идеального одноатомного газа. Какую работу совершила эта порция газа на изобарном участке данного процесса? Ответ выразите в джоулях и округлите до целого числа.
Сначала нужно найти на графике изобарный участок. При (закон Гей-Люссака). Следовательно, то есть это прямая, проходящая через начало координат (отрезок 1–2). При этом При изобарном процессе работа газа
Один моль идеального одноатомного газа совершает циклический процесс 1-2-3-4-1, график которого показан на рисунке в координатах p-V. Из предложенного перечня выберите все верные утверждения и укажите их номера.
1) В процессе 1-2 внутренняя энергия газа увеличивается.
2) В процессе 2-3 газ совершает положительную работу.
3) В процессе 3-4 газ отдает некоторое количество теплоты.
4) В процессе 4-1 температура газа увеличивается в 4 раза.
5) Работа, совершённая газом в процессе 1-2, в 3 раза больше работы, совершённой над газом в процессе 3-4.
Внутренняя энергия идеального газа пропорциональна температуре и не зависит от давления и занимаемого газом объема:
1) Процесс 1-2 -изобарное расширение. В этом процессе (согласно уравнению состояния идеального газа ) температура увеличивается, а значит и увеличивается внутренняя энергия. Утверждение верное.
2) В осях p-V работа газа равна площади под графиком. В процессе 2-3 работа газа равна нулю. Утверждение неверное.
3) Процесс 3-4 — изобарное сжатие, температура при этом уменьшается. Утверждение верное.
4) Процесс 4-1 изохорное нагревание. Давление возрастает в 4 раза, а значит и температура возрастает в 4 раза. Утверждение верное.
5) Работа, совершённая газом в процессе 1-2, в 4 раза больше работы, совершённой над газом в процессе 3-4. Утверждение неверное.
На рисунке изображён график циклического процесса, совершаемого одним молем идеального одноатомного газа. Определите, как в процессе перехода газа из состояния 3 в состояние 1 изменяются следующие физические величины: объём газа, внутренняя энергия газа.
Для каждой величины определите соответствующий характер изменения:
Запишите в ответ цифры, расположив их в порядке, соответствующем таблице:
Процесс 3−1 является изобарным охлаждением, а значит, объем газа в этом процессе уменьшается.
Внутренняя энергия газа является функцией температуры а значит, уменьшение температуры приведет к уменьшению внутренней энергии.
На рисунке изображён график процесса 1−2−3, совершаемого с пятью молями идеального одноатомного газа.
Выберите все верные утверждения относительно проведённого процесса.
1) Участок 1−2 представляет собой изотермическое сжатие.
2) На участке 2−3 температура газа увеличивается.
3) В состоянии 1 плотность газа минимальна.
4) В состоянии 3 концентрация молекул газа максимальна.
5) В состоянии 3 среднеквадратичная скорость молекул газа имеет максимальное значение.
2) Неверно. На участке 2−3 происходит изобарное сжатие. Значит, температура уменьшается.
3) Верно. При неизменной массе плотность обратно пропорциональна объему. Из графика следует, что в точке 1 объем максимальный, следовательно, плотность минимальна.
4) Верно. При неизменном числе молекул зависимость концентрации от объема обратно пропорциональна. В точке 3 объем минимальный, значит, концентрация максимальна.
5) Неверно. Из основного уравнения МКТ идеального газа
На рисунке изображён график процесса 1−2−3, совершаемого с пятью молями идеального одноатомного газа.
Выберите все верные утверждения относительно проведённого процесса.
1) На участке 1−2 температура газа увеличивается.
2) На участке 2−3 температура газа уменьшается.
3) В состоянии 1 плотность газа максимальна.
4) В состоянии 2 концентрация молекул газа максимальна.
5) В состоянии 3 среднеквадратичная скорость молекул имеет минимальное значение.
2) Верно. На участке 2-3 происходит изобарное сжатие. Значит, температура уменьшается.
3) Неверно. При неизменной массе плотность обратно пропорциональна объему. Из графика следует, что в точке 1 объем максимальный, следовательно, плотность минимальна.
4) Неверно. При неизменном числе молекул зависимость концентрации от объема обратно пропорциональна. В точке 2 объем не максимальный, значит, концентрация не максимальна.
5) Верно. Из основного уравнения МКТ идеального газа
Аналоги к заданию № 24100: 24153 Все
В тепловой машине один моль идеального одноатомного газа совершает процесс, изображенный на рисунке 1. Этот циклический процесс заменяют на другой, изображенный на рисунке 2, не изменяя ни газ, ни его количество. Как в результате изменятся следующие физические величины: передаваемое газу от нагревателя количество теплоты; совершаемая машиной механическая работа; КПД тепловой машины?
А) передаваемое газу от нагревателя количество теплоты за цикл
Б) совершаемая машиной механическая работа за цикл
Совершаемой за цикл тепловой машиной механической работе на диаграмме соответствует площадь цикла. Из диаграмм видно, что площадь обоих циклов одинаковая: Следовательно, совершаемая машиной механическая работа за цикл не изменяется (Б — 3).
Определить, что произойдёт с передаваемым газу от нагревателя количеством теплоты за цикл, немного сложнее. Подробно разберём оба цикла. На участках 1-2-3 объём газа увеличивается, его температура тоже увеличивается. Следовательно, по первому началу термодинамики, на этих участках тепло передаётся газу от нагревателя. На участках 3-4-1 температура и объём газа уменьшаются, а значит, тепло отводится от системы. Определим, сколько тепла передается газу на участках 1-2-3 (для этого потребуются первое начало термодинамики и уравнение Клапейрона — Менделеева). Для первого цикла:
Таким образом, передаваемое газу от нагревателя тепло за цикл увеличивается (А — 1).
Наконец, КПД тепловой машины связано с работой за цикл и передаваемым газу теплом от нагревателя соотношением Поскольку в результате изменения цикла работа газа не изменяется, а передаваемое от нагревателя количество теплоты увеличивается, заключаем, что КПД тепловой машины уменьшается (В — 2).
Почему при расчете Q1 работа газа вычисляется так? Ведь по графику площадь равна (4p — p)*(2V — V)
Тот же самый вопрос про Q2
При подсчете переданного газу количества теплоты необходимо сложить проделанную газом работу и изменение его внутренней энергии. Работа равна площади под процессом 1-2-3, как именно газ отдавал тепло на участке 3-4-1 не важно. От этого будет зависеть только полезна работа и отданное тепло.
Здравствуйте! Работа вроде считается по площади под фигурой, а КПД по площади фигуры? Если так, то получается, что работа увеличилась,а КПД не изменилось.
Совсем не так. Полезная работа за цикл — это площадь фигуры. КПД — это отношение полезной работы к переданному теплу. Для поиска КПД помимо подсчета площади нужно еще разобраться с тем, сколько тепла было подведено к системе. Это достаточно подробно описано в решении. Постарайтесь разобраться.
Добрый день. В последнем абзаце написано, что работа газа не меняется. А при вычислении передаваемого газу количества теплоты в формуле написано, что работа газа в первом цикле 4pV, а во втором 6pV. В чем я ошибаюсь, не могу понять.
Это работы на участке 2-3. За весь цикл работы одинаковы:
В тепловой машине один моль идеального одноатомного газа совершает процесс, изображенный на рисунке 1. Этот циклический процесс заменяют на другой, изображенный на рисунке 2, не изменяя ни газ, ни его количество. Как в результате изменятся следующие физические величины: передаваемое газу от нагревателя количество теплоты; совершаемая машиной механическая работа; КПД тепловой машины?
А) Передаваемое газу от нагревателя количество теплоты за цикл
Б) Совершаемая машиной механическая работа за цикл
Совершаемой за цикл тепловой машиной механической работе на диаграмме соответствует площадь цикла. Из диаграмм видно, что площадь обоих циклов одинаковая: Следовательно, совершаемая машиной механическая работа за цикл не изменяется (Б — 3).
Определить, что произойдет с передаваемым газу от нагревателя количеством теплоты за цикл, немного сложнее. Подробно разберем оба цикла. На участках 1-2-3 объем газа увеличивается, его температура тоже увеличивается. Следовательно, по первому началу термодинамики, на этих участках тепло передается газу от нагревателя. На участках 3-4-1 температура и объем газа уменьшаются, а значит, тепло отводится от системы. Определим, сколько тепла передается газу на участках 1-2-3 (для этого потребуются первое начало термодинамики и уравнение Клапейрона — Менделеева). Для первого цикла:
Таким образом, передаваемое газу от нагревателя тепло за цикл уменьшается (А — 2).
Наконец, КПД тепловой машины связано с работой за цикл и передаваемым газу теплом от нагревателя соотношением Поскольку в результате изменения цикла работа газа не изменяется, а передаваемое от нагревателя количество теплоты уменьшается, заключаем, что КПД тепловой машины увеличивается (В — 1).
На pV–диаграмме изображены три циклических процесса А, В и С, совершаемых одним молем идеального одноатомного газа. Обход каждого цикла на диаграмме совершается в направлении часовой стрелки.
Выберите все верные утверждения.
1) Максимальная работа совершается газом в цикле В.
2) Процесс 6–7 является адиабатическим расширением.
3) КПД цикла А равен КПД цикла С.
5) Изменение внутренней энергии в цикле В равно изменению внутренней энергии в цикле А.
1. Верно. Работу газа можно найти как площадь фигуры в (p-V):
2. Неверно. При адиабатном расширении зависимость p(V) не является линейной.
3. Неверно. КПД цикла определяется по формуле Из первого пункта следует, что работа в циклах А и С одинаковая. В цикле А газ получает теплоту на участках 1-2 и 2-3 при изобарном расширении. В цикле С газ получает теплоту на участке 5-6 (такую же, как на участке 1-2), на участке 6-7 сначала получает теплоту, а затем отдаёт. Очевидно, что теплота, полученная в цикле А, не равна теплоте, полученной в цикле С, потому КПД этих циклов не равны.
Ускоренная подготовка к ЕГЭ с репетиторами Учи.Дома. Записывайтесь на бесплатное занятие!

-->

Задание 27 № 29045
В теплоизолированном цилиндре объёмом V = 20 л под поршнем находится 1 моль идеального одноатомного газа — неона — под давлением p = 10 5 Па. Затем поршень сдвигается, и над газом совершается работа A = 500 кДж. Найдите изменение среднеквадратичной скорости теплового движения атомов аргона в данном процессе.
1. Согласно уравнению состояния Менделеева-Клапейрона и выражению для внутренней энергии U1 одного моля идеального одноатомного газа при температуре T1 имеем:
2. Поскольку средняя кинетическая энергия теплового движения атомов одноатомного газа
то в начальном состоянии газа неона
3. Подставляя численные данные из условия, получаем:
4. Газ в цилиндре под поршнем теплоизолирован, поэтому в рассматриваемом адиабатическом процессе согласно первому закону термодинамики откуда
5. В конечном состоянии неона
6. Подставляя численные данные из условия, получаем:
7. Таким образом,
I) записаны положения теории и физические законы, закономерности, применение которых необходимо для решения задачи выбранным способом (в данном случае — уравнение Менделеева-Клапейрона, выражения для внутренней энергии идеального одноатомного газа, выражение для средней кинетической энергии теплового движения атомов одноатомного газа, первый закон термодинамики для адиабатического процесса):
II) описаны все вводимые в решение буквенные обозначения физических величин (за исключением, возможно, обозначений констант, указанных в варианте КИМ, и обозначений, используемых в условии задачи):
Записи, соответствующие одному или обоим пунктам: II и III -представлены не в полном объёме или отсутствуют.
При ПОЛНОМ правильном решении лишние записи, не входящие в решение (возможно, неверные), не отделены от решения (не зачёркнуты, не заключены в скобки, рамку и т. п.).
При ПОЛНОМ решении в необходимых математических преобразованиях или вычислениях допущены ошибки, и (или) преобразования/вычисления не доведены до конца.
В решении отсутствует ОДНА из исходных формул, необходимая для решения задачи (или утверждение, лежащее в основе решения), но присутствуют логически верные преобразования с имеющимися формулами, направленные на решение задачи.
Газ находится в цилиндре под поршнем нагрели при постоянном давлении

2021-06-03
Газообразный гелий находится в цилиндре под подвижным поршнем. Газ нагревают при постоянном давлении, переводя его из состояния 1 в состояние 2 (рис.). При этом газ совершает работу $A_ $. Затем газ сжимается в процессе 2-3, ког да его давление $p$ прямо пропорционально объему $V$. При этом над газом совершается работа $A_ $ ( $A_ > 0$ ). Наконец, газ сжимается в адиабатическом процессе 3-1, возвращаясь в первоначальное состояние. Найдите работу сжатия $A_ $, совершенную над газом в адиабатическом процессе.
Обозначим температуру гелия в состояниях 1 и 2 через $T_ $ и $T_ $, а объемы газа — через $V_ $ и $V_ $. Пусть давление на изобаре 1-2 равно $p_ $, тогда работа, совершенная газом в этом процессе, будет равна
где $\nu$ — число молей гелия.
Работу, совершенную над газом на участке 2-3, можно записать в виде
где $V_ , p_ $ — объем и давление газа в состоянии 2, a $V_ , p_ $ — объем и давление в состоянии 3. На $pV$ — диаграмме точки 2 и 3 лежат на прямой, проходящей через начало координат, следовательно,
С учетом этого соотношения выражение для работы $A_ $ приобретает вид
где $T_ $ — температура гелия в состоянии 3.
Работа сжатия на адиабате 3-1 равна изменению внутренней энергии гелия:
Найдем разность температур $T_ — T_ $. Для этого перепишем выражения для $A_ $ и $A_ $ в виде
Задачи на первый закон термодинамики с решениями

Первый закон, или первое начало термодинамики является частным случаем закона сохранения энергии. Разберемся, как он работает, с помощью решения простых задач. Кстати, у нас есть и примеры решения задач на второе начало термодинамики.
Подписывайтесь на наш телеграм-канал, чтобы не только легко решать задачи, но и узнавать лайфхаки для любых жизненных ситуаций.
Первый закон термодинамики: решение задач
Алгоритм решения задач на первый закон термодинамики ничем не отличается от алгоритма решения любой другой физической задачи. С ним вы можете ознакомиться, открыв нашу универсальную памятку. Также полезно будет держать под рукой формулы, которые часто используются при решении задач.
Задача №1. Применение первого закона термодинамики
Газ находился в цилиндре с поршнем площадью поперечного сечения 200 см^2. После того, как газ нагрели, сообщив ему количество теплоты в 1,5*10^5 Дж, поршень сдвинулся на расстояние h=30 см. Как изменилась внутренняя энергия газа, если его давление осталось равным 2*10^7 Па.
Запишем первое начало термодинамики:
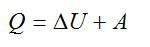
Работу против внешних сил, которую совершил газ, можно найти по формуле из механики:
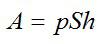
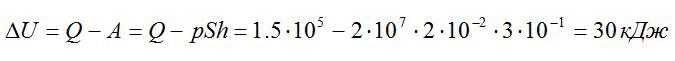
Ответ: 30 кДж.
Задача №2. Применение первого закона термодинамики
Над газом была совершена работа 55 Дж, а его внутренняя энергия увеличилась на 15 Джоулей. Какое количество теплоты получил или отдал газ в этом процессе?
Записываем первое начало термодинамики и подставляем значения:
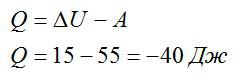
Ответ: в процессе газ отдал 40 Дж теплоты.
Задача №3. Расчет работы, изменения внутренней энергии и количества теплоты
Кислород нагрели при постоянном давлении p=80 кПа. Объем газа увеличился с 1 до 3 кубических метров. Определить изменение внутренней энергии кислорода, работу, совершенную газом, и количество теплоты, сообщенное ему.
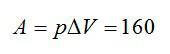
Изменение внутренней энергии равно:
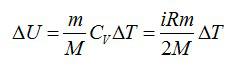
Используем уравнение состояния газа:
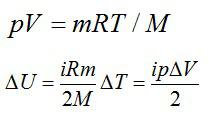
Число степеней свободы i для двухатомной молекулы равно 5.
Согласно первому закону термодинамики, сообщенное газу тепло равно:
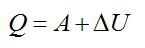
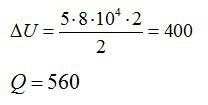
Ответ: А=160 кДж, ∆U=400 кДж, Q=560 кДж.
Задача №4. Изопроцессы
Газ находится в баллоне при температуре 400 К. До какой температуры нужно нагреть газ, чтобы его давление увеличилось в 1,5 раза?
Так как нагревание газа происходит при постоянном объеме, процесс – изохорный. При изохорном процессе:
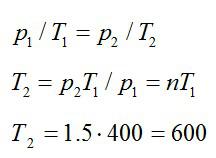
Ответ: 600 К.
Задача №5. Расчет изменения энтропии
Найти изменение ∆S энтропии при расширении массы m = 6 г гелия от объема V1 = 20 л под давлением р1 = 150 кПа к объему V2 = 60 л под давлением р2 = 100 кПа.
Изменение энтропии при переходе вещества из состояния 1 в состояние 2:
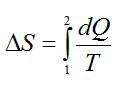
Согласно первому началу термодинамики:
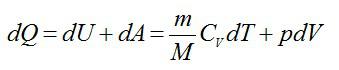
Из уравнения Менделеева-Клапейрона выразим давление:
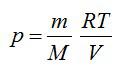
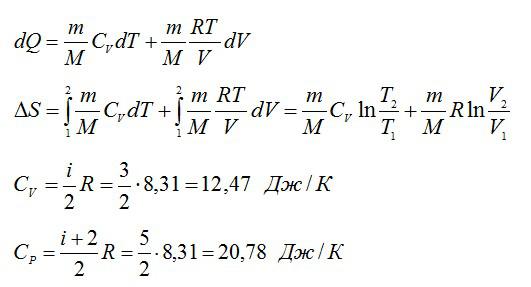
Из уравнения Менделеева-Клапейрона:
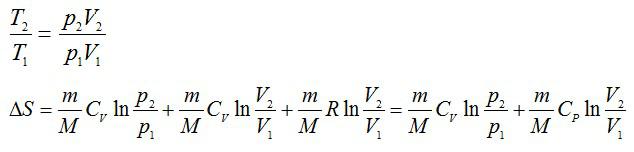
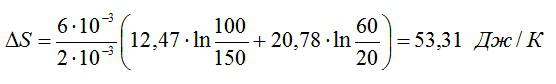
Кстати! Для наших читателей действует скидка 10% на любой вид работы.
Вопрос 1. Приведите пример действия первого закона термодинамики.
Ответ. В качестве примера можно привести газ в сосуде. Если сообщить ему какое-то количество теплоты, оно пойдет на увеличение внутренней энергии газа в сосуде.
Вопрос 2. Сформулируйте первый закон термодинамики.
Ответ. В любой изолированной системе запас энергии остается постоянным.
Вопрос 3. Как еще можно сформулировать первый закон термодинамики?
Ответ. Вот разные формулировки первого закона термодинамики:
- Количество теплоты, полученное системой, идет на изменение внутренней энергии системы, а также на совершение работы против внешних сил.
- Невозможен вечный двигатель первого рода (двигатель, совершающий работу без затраты энергии).
Вопрос 4. Что такое изопроцесс? Какие есть изопроцессы?
Изопроцесс – это термодинамический процесс, при котором один из параметров системы (давление, объем, температура, энтропия) остается неизменным.
- изотермическим (T=const);
- изобарным (P=const);
- изохорным (V=const);
- Адиабатическим (отсутствует теплообмен с окружающей средой).
Вопрос 5. При каком изопроцессе газ не совершает работу?
Ответ. При изохорном.
Ищете, где почитать теорию по теме, а учебника нет под рукой? Далеко ходить на надо, почитайте наш отдельный материал по первому началу термодинамики. А если при решении заданий понадобится помощь, обращайтесь в профессиональный студенческий сервис.
Иван Колобков, известный также как Джони. Маркетолог, аналитик и копирайтер компании Zaochnik. Подающий надежды молодой писатель. Питает любовь к физике, раритетным вещам и творчеству Ч. Буковски.
Газ находится в цилиндре под поршнем нагрели при постоянном давлении
Тонкостенный цилиндр с воздухом закрыт снизу поршнем массой m = 1 кг, который может без трения перемещаться в цилиндре. Цилиндр плавает в вертикальном положении в воде при температуре T = 293 К (см. рис.). Когда цилиндр опустили при постоянной температуре на глубину h = 1 м (от поверхности воды до его верхней крышки), он потерял плавучесть. Какое количество воздуха было в цилиндре? Атмосферное давление равно p = 10 5 Па, масса цилиндра и воздуха в цилиндре гораздо меньше массы поршня.
Поскольку цилиндр лёгкий, а трения между ним и поршнем нет, то при плавании воздух в цилиндре находится под атмосферным давлением Обозначим объём воздуха в цилиндре при плавании через Тогда, согласно уравнению Клапейрона — Менделеева, где — искомое количество воздуха.
Неизвестный объём воздуха при атмосферном давлении можно найти из следующих соображений. Сила Архимеда, действующая на цилиндр с поршнем при его плавании и в момент потери плавучести, одна и та же и равна весу поршня: где — плотность воды, а — объём вытесненной воды, равный объёму воздуха в цилиндре в момент потери плавучести. Согласно закону Бойля — Мариотта, при изотермическом процессе Давление в цилиндре равно, согласно формуле для давления в жидкости, покоящейся в ИСО, и условию равновесия тела (сумма сил равна нулю),
ЗАМЕЧАНИЕ: давление воды определяется глубиной погружения нижней поверхности поршня,ПОЭТОМУ
ИЗМЕНИТЬ в условии задачи
«Когда цилиндр опустили при постоянной температуре на глубину h = 1 м (от поверхности воды до его верхней крышки), . «
«Когда цилиндр при постоянной температуре полностью погрузили в воду и нижняя поверхность поршня оказалась на глубине h = 1 м от поверхности воды, . «
НА РИСУНКЕ ИЗМЕНИТЬ размер двойной стрелки (h)
Давление воды на верхнюю крышку равно давлению газа, поскольку цилиндр невесомый.
Давление воды на поршень (оно больше из-за большей глубины) равно давлению газа плюс давление поршня.
Почему давление в цилиндре равно атмосферному.
На верхнюю поверхность цилиндра действуют силы давления внешнего воздуха и внутреннего воздуха Сил на верхнюю поверхность со стороны стенок нет, поскольку: а) цилиндр невесом; б) стенки вертикальны, и поэтому силы давления воды на боковую поверхность компенсируют друг друга; в) трения между поршнем и цилиндром нет. Поскольку (опять же) цилиндр невесом, силы давления равны:
В вертикальном цилиндре под тяжёлым горизонтальным поршнем площадью 0,2 м 2 находится идеальный газ. Атмосферное давление над поршнем равно 10 5 Па, а под поршнем – на 20% выше. Газ медленно нагревают, в результате чего поршень поднимается на высоту 10 см. Какую работу при этом совершает газ?
Давление под поршнем до и после нагрева одинаково. Тогда работа идеального газа равна:
В вертикальном цилиндре под тяжёлым горизонтальным поршнем площадью 0,1 м 2 находится идеальный газ. Атмосферное давление над поршнем равно 10 5 Па, а под поршнем — на 30% выше. Газ медленно нагревают, в результате чего поршень поднимается на высоту 20 см. Какую работу при этом совершает газ? Ответ дайте в джоулях.
В процессе нагревания давление под поршнем остаётся постоянным, т. е. процесс является изобарическим. Тогда работа идеального газа равна:
В горизонтальном цилиндре с гладкими стенками под массивным поршнем с площадью S находится одноатомный идеальный газ. Поршень соединён с основанием цилиндра пружиной с жёсткостью k. В начальном состоянии расстояние между поршнем и основанием цилиндра равно L, а давление газа в цилиндре равно внешнему атмосферному давлению p (см. рисунок). Какое количество теплоты Q передано затем газу, если в результате поршень медленно переместился вправо на расстояние b?
Тепло, переданное газу, идёт на изменение его внутренней энергии и на совершением им работы:
В начальном состоянии давление и объём газа равны и в конечном состоянии — и Используя уравнение Менделеева — Клапейрона для изменения внутренней энергии получаем:
Чтобы рассчитать работу, заметим, что в каждый момент времени, когда поршень сдвинут на от начального положения давление равно т. е. давление линейно зависит от объёма. Значит, на pV-диаграмме процесс расширения будет изображён отрезком прямой, а фигура под графиком будет являться трапецией, площадь которой равна
Заметим, что этот результат можно получить, посчитав работу газа как минус сумму работ пружины и внешней атмосферы
В условии сказано, что поршень медленно переместился. Это означает что процесс изотермический, не так ли?
Нет, температура не постоянна. Медленность нужна, чтобы успевать передавать тепло. Очень быстрый процесс был бы адиабатическим.
Здравствуйте. Почему в задаче 7129 постоянное давление в работе, а в этой нет?
В задаче 7129 давление постоянно, так как внешнее (атмосферное) давление и сила трения постоянны. В этой задаче атмосферное давление также постоянно, а вот сила натяжения пружины не постоянна, она увеличивается при расширении газа из-за удлинения пружины.
Таким образом, а удельная теплоёмкость газа в данном изобарическом процессе равна по определению:
Поскольку в изобарическом процессе получаем:
В цилиндре под поршнем при комнатной температуре t долгое время находится только вода и её пар. Масса жидкости в два раза больше массы пара. Первоначальное состояние системы показано точкой на pV-диаграмме. Медленно перемещая поршень, объём V под поршнем изотермически увеличивают от V до 6V . Постройте график зависимости давления p в цилиндре от объёма V на отрезке от V до 6V . Укажите, какими закономерностями вы при этом воспользовались.
1. На участке от до давление под поршнем постоянно (давление насыщенного пара на изотерме). На участке от до давление под поршнем подчиняется закону Бойля — Мариотта.
На участке от до график — горизонтальный отрезок прямой, на участке от до — фрагмент гиперболы (для экспертов: отсутствие названий не снижает оценку, названия помогают оценке графика, сделанного от руки).
2. В начальном состоянии над водой находится насыщенный водяной пар, так как за длительное время в системе установилось термодинамическое равновесие.
3. Пока в цилиндре остается вода, при медленном изотермическом расширении пар остается насыщенным. Поэтому график будет графиком константы, т. е. отрезком горизонтальной прямой. Количество воды в цилиндре при этом убывает. При комнатной температуре концентрация молекул воды в насыщенном паре ничтожна по сравнению с концентрацией молекул воды в жидком агрегатном состоянии. Масса воды в два раза больше массы пара. Поэтому, во-первых, в начальном состоянии насыщенный пар занимает объём, практически равный Во-вторых, чтобы вся вода испарилась, нужно объём под поршнем увеличить ещё на Таким образом, горизонтальный отрезок описывает зависимость на участке от до
4. При под поршнем уже нет жидкости, все молекулы воды образуют уже ненасыщенный водяной пар, который можно на изотерме описывать законом Бойля — Мариотта: т. е. Графиком этой зависимости служит гипербола. Таким образом, на участке от до зависимость изображается фрагментом гиперболы.
Разделы ![]()
Дополнительно

Задача по физике - 3685
Найти работу изобарического расширения $\nu = 2$ молей идеального газа, если известно, что концентрация молекул в конечном состоянии в $q = 2$ раза меньше, чем в начальном при температуре $T_ <1>= 300 К$.
Задача по физике - 3687
Один моль идеального газа изохорически перевели из состояния 1 в состояние 2 так, что его давление уменьшилось в $n = 1,5$ раза. Затем газ изобарически нагрели до первоначальной температуры $T_<1>$. При этом газ совершил работу $A = 0,83 кДж$. Определите величину $T_<1>$.
Задача по физике - 3688
В теплоизолированном цилиндре под теплонепроницаемым поршнем находится одноатомный идеальный газ с начальным давлением $p_ <0>= 10^ Па$, объемом $V_ <0>= 3 дм^$ и температурой $T_ <0>= 300 К$. При сжатии газа над ним совершили работу $A = 90 Дж$. Найдите температуру газа после сжатия.
Задача по физике - 3689
На сколько увеличится внутренняя энергия одноатомного идеального газа в процессе изобарического расширения, если газу сообщили при этом количество теплоты $Q = 30 кДж$?
Задача по физике - 3690
Некоторое количество идеального одноатомного газа участвует в процессе, в ходе которого сначала давление газа изохорически увеличили $n = 2$ раза, а затем его объем изобарически увеличили в $k = 3$ раза. Какое количество теплоты сообщают газу в указанном процессе? Начальное давление и объем газа $p_ <0>= 10^ Па$ и $V_ <0>= 100 л$ соответственно.
Задача по физике - 3691
Водород массой $m = 0,5 кг$ участвует в процессе, в ходе которого сначала его давление изохорически уменьшают в $n = 5$ раз, а затем его объем изобарически увеличивают таким образом, что начальная и конечная температуры газа в процессе совпадают. Молярная масса водорода $\mu = 2 г/моль$. Какую работу совершил газ в указанном процессе, если его начальная температура $T_ <0>= 500 К$?
Задача по физике - 3692
При изобарном расширении $m = 20 г$ водорода его объем увеличился в $n = 2$ раза. Начальная температура газа $T = 300 К$. Определите работу газа при расширении. Молярная масса водорода $\mu = 2 г/моль$.
Задача по физике - 3693
В теплоизолированный цилиндрический сосуд, закрытый легко перемещающимся практически невесомым поршнем, поместили $\nu$ молей атомарного газа при температуре $T_<0>$. Начальный объем газа — $V_<0>$. В результате поршень двигается до тех пор, пока объем газа не увеличится до $V$. Во сколько раз уменьшилась при этом температура газа, если давление окружающей среды остается постоянным. Газ — идеальный.
Задача по физике - 3694
Один моль одноатомного газа, имевшего температуру $0^ < \circ>С$, нагревается при постоянном давлении. Какое количество теплоты необходимо сообщить газу, чтобы его объем удвоился? Какая работа при этом будет совершена газом?
Задача по физике - 3695
В теплоизолированный сосуд поместили $\nu_<1>$ молей атомарного газа при температуре $T_<1>$ и $\nu_$ молей при температуре $T_$. Определить установившуюся температуру газа. Газ — идеальный.
Задача по физике - 3696
Считая известной молярную теплоемкость газа при постоянном объеме $c_
a) $p = \frac< \alpha >$;
б) $V = \frac< \alpha>$;
в) $V = \alpha T^$;
г) $p = \alpha V$.
В этих формулах $p, V, T$ — давление, объем и температура (по абсолютной шкале) газа соответственно; $\alpha$ — некоторая изначально заданная константа.
Задача по физике - 3697
Один моль идеального одноатомного газа участвует в термодинамическом процессе, для которого его теплоемкость меняется по закону $c = R(T_<0>^ / T^)$, где $T_ <0>= 300 К$. При какой температуре объем газа будет максимальным?
Задача по физике - 3698
Один моль идеального одноатомного газа участвует в термодинамическом процессе, для которого его теплоемкость меняется по закону $c = R (T_<0>/T), T_ <0>= 400 К$. При какой температуре давление газа будет минимальным?
Задача по физике - 3699
В двух объемах находится: в одном $N_ <1>= 10^$, а в другом $N_ = 0,4 \cdot 10^$ молекул одного и того же газа. В исходном состоянии внутренняя энергия первого объема газа была на $\Delta U = 1,9 Дж$ больше, второго. Объемы приводят в тепловой контакт. В установившемся состоянии средняя энергия, приходящаяся на одну молекул в первом объеме уменьшилась на 25 %. Какова внутренняя энергия газа в первом объеме в исходном состоянии? Газ — идеальный. Теплообмен с внешней средой отсутствует.
Задача по физике - 3700
В тающий снег поместили пробирку со льдом, имеющим температуру $0^ < \circ>С$. Будет ли таять лед в пробирке?
Читайте также:

